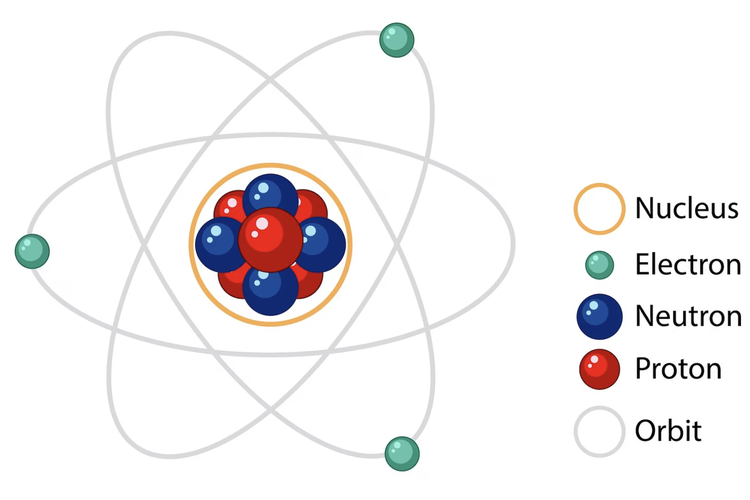
rsudkotabandung.web.id – Struktur atom merupakan salah satu konsep dasar dalam ilmu kimia yang harus dipahami dengan baik. Pemahaman mengenai struktur atom sangat penting karena menjadi dasar dari banyak konsep lainnya, seperti konfigurasi elektron, sifat periodik unsur, dan ikatan kimia. Artikel ini akan menyajikan beberapa contoh soal struktur atom beserta jawabannya secara lengkap dan terstruktur untuk membantu pembelajaran.
Contoh Soal Struktur Atom beserta Jawabannya
Berikut beberapa contoh soal struktur atom beserta jawabannya, Simak baik-baik!
Soal 1: Menentukan Jumlah Partikel Penyusun Atom
Berapa jumlah proton, neutron, dan elektron dalam atom karbon-12 (C-12)?
Jawaban:
Atom karbon mempunyai nomor atom 6, yang berarti mempunyai 6 proton. Karbon-12 menunjukkan bahwa nomor massanya adalah 12. Oleh karena itu:
- Jumlah proton = 6
- Jumlah neutron = Nomor massa – Nomor atom = 12 – 6 = 6
- Jumlah elektron (untuk atom netral) = Jumlah proton = 6
Jadi, atom karbon-12 memiliki 6 proton, 6 neutron, dan 6 elektron.
Soal 2: Konfigurasi Elektron
Tuliskan konfigurasi elektron dari atom oksigen (O) yang memiliki nomor atom 8.
Jawaban:
Nomor atom oksigen adalah 8, yang berarti memiliki 8 elektron. Konfigurasi elektron dimulai dari kulit dengan tingkat energi terendah (kulit K) ke tingkat energi yang lebih tinggi (kulit L), dan seterusnya.
Kulit K dapat menampung maksimal 2 elektron.
Kulit L dapat menampung maksimal 8 elektron.
Distribusi elektronnya adalah:
Kulit K: 2 elektron dan kulit L: 6 elektron
Jadi, konfigurasi elektronnya adalah 2, 6.
Soal 3: Menentukan Nomor Massa
Unsur natrium (Na) memiliki nomor atom 11 dan memiliki 12 neutron. Berapakah nomor massanya?
Jawaban:
Nomor massa (A) adalah jumlah proton ditambah jumlah neutron.
Nomor atom (jumlah proton) = 11
Jumlah neutron = 12
Nomor massa = 11 + 12 = 23
Jadi, nomor massa unsur natrium adalah 23.
Soal 4: Identifikasi Isotop
Sebutkan isotop dari unsur hidrogen dan jelaskan perbedaannya.
Jawaban:
Hidrogen memiliki tiga isotop utama, yaitu:
Protium (¹H): Tidak memiliki neutron, hanya memiliki 1 proton.
Deuterium (²H): Memiliki 1 proton dan 1 neutron.
Tritium (³H): Memiliki 1 proton dan 2 neutron.
Perbedaannya terletak pada jumlah neutron dalam inti atom, sementara jumlah proton (nomor atom) tetap sama yaitu 1.
Soal 5: Menentukan Elektron Valensi
Berapa jumlah elektron valensi pada atom fosfor (P) yang memiliki nomor atom 15?
Jawaban:
Nomor atom fosfor adalah 15, yang berarti memiliki 15 elektron. Konfigurasi elektronnya adalah:
- Kulit K: 2 elektron, kulit L: 8 elektron, dan kulit M: 5 elektron
Elektron valensi adalah elektron yang berada pada kulit terluar. Jadi, jumlah elektron valensi pada atom fosfor adalah 5.
Soal 6: Menentukan Nomor Atom dari Ion
Ion X²⁻ memiliki 18 elektron. Tentukan nomor atom dari unsur X.
Jawaban:
Ion X²⁻ memiliki dua elektron lebih banyak daripada atom netralnya. Jadi, atom netral dari unsur X memiliki 18 – 2 = 16 elektron. Karena jumlah elektron sama dengan jumlah proton pada atom netral, nomor atom X adalah 16, yang berarti unsur tersebut adalah belerang (S).
Soal 7: Menentukan Elektron pada Isotop
Berapa jumlah elektron dalam ion klorida (Cl⁻) dengan nomor massa 35?
Jawaban:
Unsur klorin (Cl) memiliki nomor atom 17, yang berarti atom netral klorin memiliki 17 elektron. Ion klorida (Cl⁻) memiliki satu elektron lebih banyak, sehingga jumlah elektronnya adalah 17 + 1 = 18.
Soal 8: Menentukan Isotop Stabil
Dari dua isotop karbon, karbon-12 dan karbon-14, manakah yang lebih stabil dan mengapa?
Jawaban:
Karbon-12 (C-12) lebih stabil dibandingkan karbon-14 (C-14). Karbon-12 memiliki 6 proton dan 6 neutron, yang merupakan kombinasi yang sangat stabil secara energi. Karbon-14, di sisi lain, memiliki 6 proton dan 8 neutron, yang membuatnya radioaktif dan mengalami peluruhan beta untuk mencapai stabilitas.
Soal 9: Menentukan Jumlah Neutron
Berapa jumlah neutron dalam isotop uranium-238 (²³⁸U)?
Jawaban:
Nomor massa uranium-238 adalah 238, dan nomor atomnya adalah 92 (jumlah proton). Jumlah neutron bisa dihitung dengan mengurangkan nomor atom dari nomor massa:
Jumlah neutron = Nomor massa – Nomor atom = 238 – 92 = 146
Jadi, jumlah neutron dalam isotop uranium-238 adalah 146.
Soal 10: Menentukan Elektron dalam Ion
Berapa jumlah elektron dalam ion Fe³⁺ dengan nomor atom 26?
Jawaban:
Atom besi (Fe) memiliki nomor atom 26, yang berarti atom netral besi memiliki 26 elektron. Ion Fe³⁺ berarti atom besi telah kehilangan 3 elektron. Jumlah elektronnya adalah:
Jumlah elektron = 26 – 3 = 23
Jadi, ion Fe³⁺ memiliki 23 elektron.
Soal 11: Menentukan Nomor Massa dari Ion
Jika ion sulfur (S²⁻) memiliki 16 proton dan 18 elektron, berapa nomor massanya jika memiliki 16 neutron?
Jawaban:
Nomor massa adalah jumlah proton dan neutron. Untuk ion sulfur ini:
Jumlah proton = 16
Jumlah neutron = 16
Nomor massa = Jumlah proton + Jumlah neutron = 16 + 16 = 32
Jadi, nomor massa dari ion sulfur tersebut adalah 32.
Soal 12: Menentukan Jumlah Elektron Valensi
Berapa jumlah elektron valensi pada atom klor (Cl) yang memiliki nomor atom 17?
Jawaban:
Nomor atom klor adalah 17, sehingga konfigurasi dari elektronnya adalah:
- Kulit K: 2 elektron, kulit L: 8 elektron, kulit M: 7 elektron
Elektron valensi adalah elektron yang berada pada kulit terluar. Jadi, jumlah elektron valensi pada atom klor adalah 7.
Soal 13: Menentukan Konfigurasi Elektron untuk Ion
Tuliskan konfigurasi elektron dari ion Al³⁺ yang memiliki nomor atom 13.
Jawaban:
Nomor atom aluminium adalah 13, yang berarti atom netral aluminium memiliki 13 elektron. Konfigurasi elektron dari atom netral aluminium adalah:
- Kulit K: 2 elektron, kulit L: 8 elektron, dan kulit M: 3 elektron
Ion Al³⁺ telah kehilangan 3 elektron, sehingga konfigurasi elektronnya adalah:
- Kemudian, Kulit K: 2 elektron dan kulit L: 8 elektron
Jadi, konfigurasi elektron dari ion Al³⁺ adalah 2, 8.
Soal 14: Menentukan Nomor Atom dari Isotop
Isotop X memiliki 20 neutron dan nomor massa 39. Berapakah nomor atomnya dan unsur apakah itu?
Kemudian, jawabannya:
Nomor massa adalah jumlah proton dan neutron. Untuk isotop ini:
Nomor massa = 39
Jumlah neutron = 20
Jumlah proton (nomor atom) = Nomor massa – Jumlah neutron = 39 – 20 = 19
Nomor atom 19 menunjukkan bahwa unsur tersebut adalah kalium (K). Jadi, nomor atomnya adalah 19 dan unsur tersebut adalah kalium.
Soal 15: Menentukan Konfigurasi Elektron dari Isotop
Tuliskan konfigurasi elektron dari isotop nitrogen-15 (N-15) dengan nomor atom 7.
Kemudian, jawabannya:
Nomor atom nitrogen adalah 7, yang berarti atom netral nitrogen memiliki 7 elektron. Konfigurasi elektronnya adalah:
- Kulit K: 2 elektron dan kulit L: 5 elektron
Nomor massa 15 tidak mempengaruhi konfigurasi elektron karena berkaitan dengan jumlah neutron. Jadi, konfigurasi elektron dari isotop nitrogen-15 adalah 2, 5.
Kesimpulan
Dengan memahami berbagai contoh soal struktur atom beserta jawabannya, kita dapat lebih mendalami konsep-konsep dasar yang menjadi fondasi ilmu kimia. Setiap soal memberikan gambaran praktis tentang bagaimana prinsip-prinsip tersebut diterapkan dalam konteks nyata. Semoga artikel ini membantu memperluas pemahaman kamu dan meningkatkan keterampilan dalam memecahkan soal-soal struktur atom. Selamat belajar dan terus berlatih!